저번 1-1편에서..
빠른 반응 속도를 이야기하는데 왜 ‘빛’이 필요하지?
라는 질문에 답하기 위한 빌드업을 했었습니다. 그 빌드업 내용을 요약하면 아래와 같습니다.
화학은 물질의 특성과 변화, 화학반응을 연구하는 학문이다.
화학반응의 반응 속도는 주어진 조건의 농도와 고유 빠르기에 따라 결정된다
주어진 조건에서 변화의 고유한 빠르기 비율이 평형 지점을 결정하며 그것이 자연의 방향성이다.
변화의 고유한 빠르기는 온도에 영향을 받는다.
화학자들은 온도가 올라가면 반응 속도가 빨라지는 것을 경험적으로 알았지만 그 이유가 무엇인지 어떻게 설명할지 고민했습니다. 저번에 인용한 1967년 노벨 화학상 수상연설을 다시 살펴보겠습니다.
혼합물을 가열하면 거의 모든 화학반응은 더 빠르게 진행됩니다. 반트 호프와 다른 발견으로 1903년 제3회 노벨 화학상을 수상한 스반테 아레니우스는 온도에 따라 반응 속도가 어떻게 증가하는지를 설명하는 수학적 공식을 수립했습니다.
이 공식은 다음과 같은 가정을 바탕으로 해석될 수 있습니다. 두 분자가 충돌할 때 대개는 아무 일 없이 다시 멀어지지만, 충돌이 충분히 격렬할 경우 분자가 분해되고 원자들이 재결합하여 새로운 분자가 형성된다는 것입니다.
또한 이런 가능성도 생각해 볼 수 있습니다. 분자들이 서로 적당한 속도로 접근하더라도, 한 분자 내부의 원자들이 격렬하게 진동하고 있다면 그 분자가 분해되기 위해 굳이 강한 충격이 필요하지 않을 수도 있다는 것입니다.
당시에 이미 높은 온도는 두 가지, 즉 분자가 더 빠르게 움직인다는 것과 원자가 더 격렬하게 진동한다는 것을 의미한다는 사실이 알려져 있었습니다. 또한 반응 속도가 측정될 수 있는 상황이라 하더라도, 전체 충돌 중 실제로 반응으로 이어지는 것은 극히 일부에 불과하다는 사실도 이해되고 있었습니다. - Nobel Prize in Chemistry 1967 Award ceremony speech
차근차근 살펴보겠습니다. 이번 인용에서 핵심 키워드는 ‘충돌’과 ‘온도’입니다. 1-1에서 살펴본 예시는 아주 간단히 설명하기 위해서 A가 B로 혹은 B가 A로 변하는 화학반응을 예시로 들었습니다. 이번에는 C와 D가 만나 E라는 새로운 물질로 바뀌는 예시, C+D→E 를 들어보겠습니다. 만약 엄청 큰 상자에 아주 작은 C 하나 그리고 D 하나만 있다면 반응이 일어날까요? 멀리 떨어져 있는 C와 D가 갑자기 사라져서 상자 어딘가에서 E가 발생하는 일은 일어나지 않습니다. C와 D가 서로 가까이 만나야, 충돌해야 E라는 물질이 만들어질 수 있습니다. 저번에 농도가 낮으면 반응 속도가 대체로 느리다고 말씀드렸죠? 같은 맥락에서 C+D→E 와 같은 반응도 C와 D의 농도가 높으면 C와 D가 충돌할 확률이 높아져서 반응 속도가 빨라집니다.
자연스럽게 A→B 같은 반응은 충돌이 없는데 어떻게 일어나는지 궁금하실 겁니다. 만약 A라는 물질 한 개를 무한히 큰 진공 상자에 두면 반응이 일어날까요? 보통은 주변과의 충돌이 거의 없으면 반응이 매-우 느려집니다. 하지만 적당한 크기의 상자에 A 열개를 같은 조건에서 넣어 둔다면 아까보다는 더 빠른 속도로 일어날 것입니다. A라는 물질은 자유롭게 움직이면서 자연스럽게 '충돌'합니다. 그게 같은 A일 수도 있고 생긴 B일 수도 있고 벽일 수도 있습니다. 그럼 충돌’만’ 일어나면 화학반응이 일어날까요?
정답은 ‘아니오’입니다. 만약, 충돌이 화학반응의 유일한 조건이었다면, 1-1에서 말씀드렸듯이 A→B 와 B→A의 고유한 빠르기가 차이 날 이유가 없습니다. 같은 공간에서 A와 B는 충돌이 비슷한 수준으로 일어날 것이기 때문입니다. 즉, 화학반응은 충돌보다 더 중요한 조건이 또 있다는 사실을 암시합니다.
그럼 그게 '온도'냐고 물으신다면 절반짜리 정답입니다. 온도는 분명히 화학반응의 고유한 빠르기를 변화시키는 중요한 '조건'이지만 그 배경을 살펴볼 필요가 있습니다. 다시 아까 인용한 부분의 일부를 가져오겠습니다.
두 분자가 충돌할 때 대개는 아무 일 없이 다시 멀어지지만, 충돌이 충분히 격렬할 경우 분자가 분해되고 원자들이 재결합하여 새로운 분자가 형성된다는 것입니다.
또한 이런 가능성도 생각해 볼 수 있습니다. 분자들이 서로 적당한 속도로 접근하더라도, 한 분자 내부의 원자들이 격렬하게 진동하고 있다면 그 분자가 분해되기 위해 굳이 강한 충격이 필요하지 않을 수도 있다는 것입니다.
당시에 이미 높은 온도는 두 가지, 즉 분자가 더 빠르게 움직인다는 것과 원자가 더 격렬하게 진동한다는 것을 의미한다는 사실이 알려져 있었습니다. 또한 반응 속도가 측정될 수 있는 상황이라 하더라도, 전체 충돌 중 실제로 반응으로 이어지는 것은 극히 일부에 불과하다는 사실도 이해되고 있었습니다. - Nobel Prize in Chemistry 1967 Award ceremony speech
핵심은 화학반응에 수반되는 '충돌'이 격렬할 수도 있고, 적당한 속도로 접근해서 격렬하지 않을 수도 있다는 사실입니다. 상자에 A 물질 10개를 넣었다고 상상해봅시다. 상태는 기체라고 했을 때, 10개의 A들은 같은 속도로 움직이고 있을까요? 누구는 억까 당해서 충돌로 인해 에너지를 잃어 느리게 운동할 수도 있고 누구는 운이 좋아서 높은 에너지를 갖고 빠르게 운동할 수도 있습니다. 10개의 A는 각각을 살펴보면 저마다의 속도 즉, 에너지를 갖고 있습니다.
그러면 A가 10개 들어있는 상자 10개를 준비해보겠습니다. 각 상자는 독립적으로 고립된 상태입니다. 그러면 10개 중 어떤 상자는 운이 좋아 에너지가 높은 A만 잔뜩 있고 어떤 상자는 운이 나빠서 에너지가 낮은 A만 잔뜩 있을까요? 그렇지 않습니다. 각 상자가 외부와 에너지를 주고받지 않는 고립계이고 온도가 같다면, 상자 안 총에너지는 시간에 따라 보존됩니다.
그러므로 같은 에너지를 10개의 A가 각각 나눠 가져야합니다. 제일 쉽게 생각할 수 있는 방식은 N분의 1씩 균등하게 나눠 갖는 것인데 분명히 아까 저마다 각각의 속도를 가질 수 있다고 했습니다. 자연의 미시 세계는 끊임없이 충돌하며 에너지를 서로 주고 받습니다. 이 과정에서 자연은 '가장 확률이 높은 상태'를 찾아갑니다. 그럼 최종적으로 어떻게 자연은 이 에너지를 분배할까요?
아마도 한 번쯤은 '열역학 제2법칙'이나 '무질서도' 그리고 '엔트로피'라는 단어를 들어보셨을 겁니다.
볼츠만이라는 과학자는 이 에너지 분배 문제를 '무질서도가 최대'라는 관점에서 확률/통계 문제를 풀었고 그 결과 '볼츠만 확률 분포'라는 것을 수학적으로 유도했습니다. 그리고 그 분포를 바꾸는 핵심은 바로 '온도'입니다.
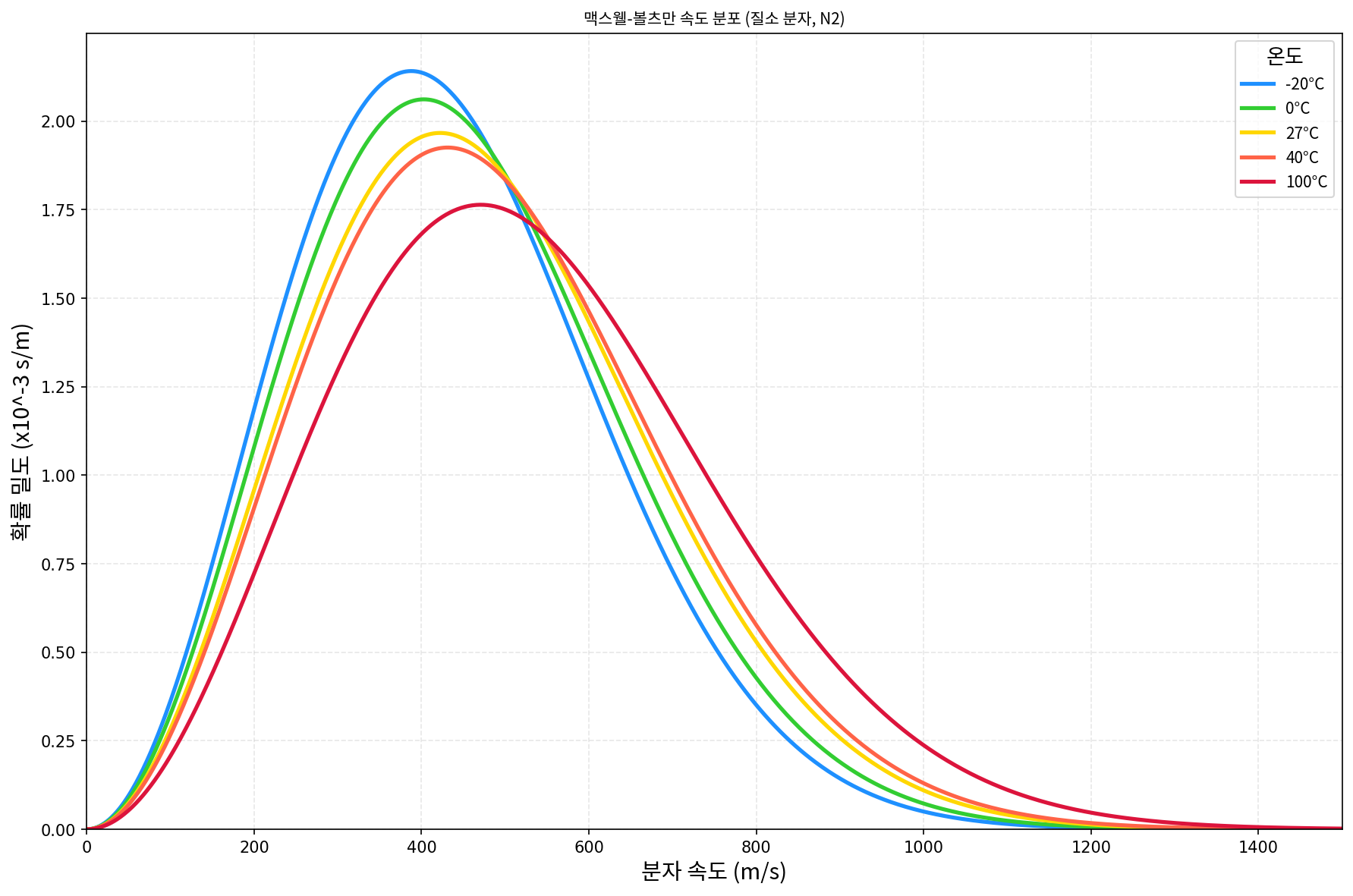
<섭씨 -20도, 0도, 27도, 40도 그리고 100도에서 맥스웰-볼츠만 분포 graph by claude>
위의 그래프에서 온도가 높을수록 분포가 조금씩 오른쪽으로 이동하는 것을 확인하실 수 있습니다. 즉, 에너지가 높은 분자의 개수가 많아진다는 뜻입니다. 온도가 낮을 때도 어떤 녀석은 빠르고 온도가 높을 때도 어떤 녀석은 ...

![[시리즈 연재] 1-1: 1967년 노벨 화학상 다루려고 했는데 1901년꺼 다룬 ssul...](https://post-image.valley.town/8_oQ-hrxIzHbTFqwCyKie.png)
![[시리즈 연재] 프롤로그](https://post-image.valley.town/rvfznnLimOm4-_eSCr9tD.png)




