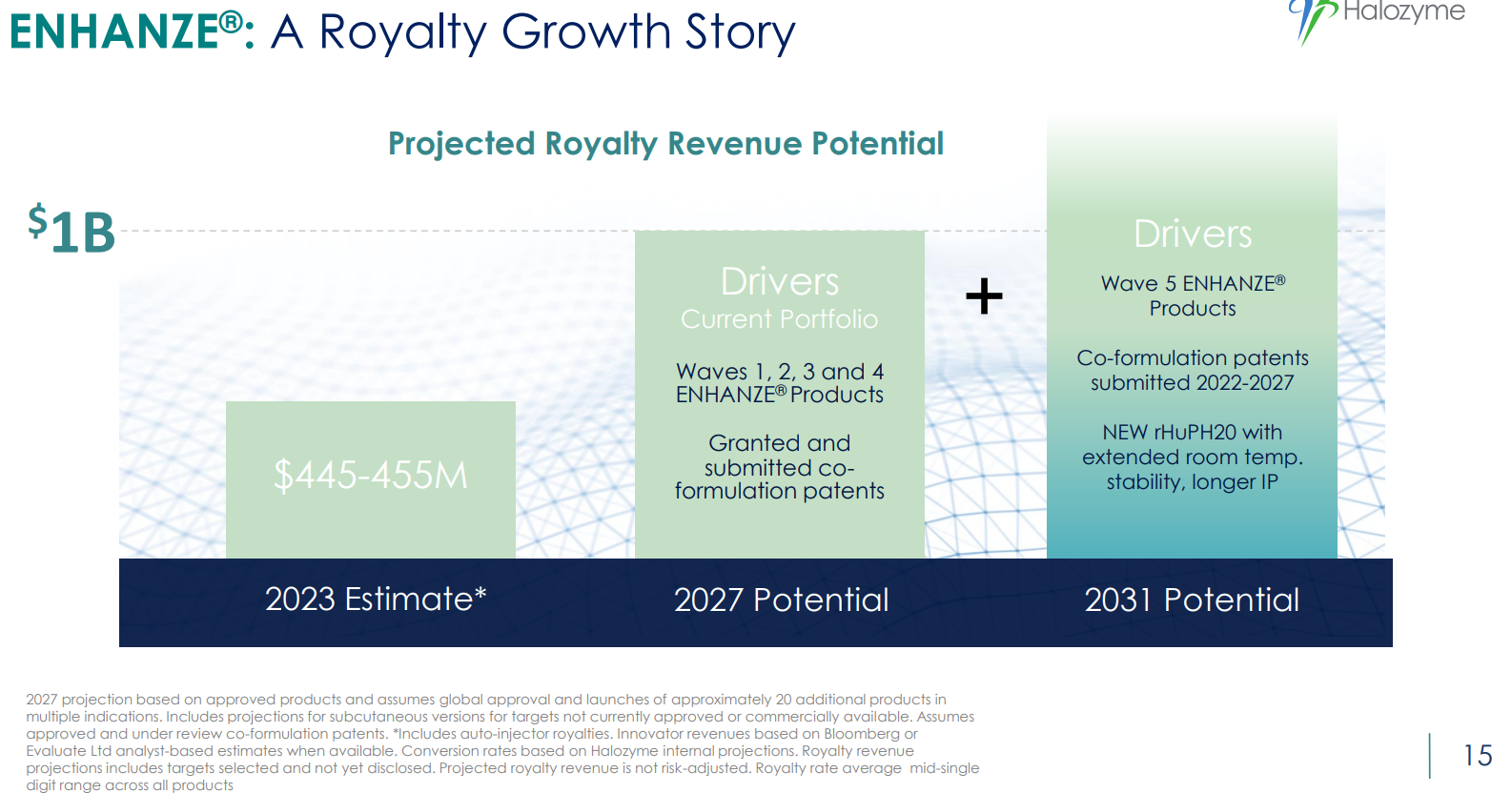
키트루다는 PD-1 억제제 계열의 면역항암제이다. 머크가 키트루다 SC의 고삐를 쥐는 이유가 있다.
이 키트루다의 라이벌인 BMS의 '옵디보' 때문이다.
해당 약품은 할로자임의 ENHANZE를 활용하여 이미 곧 SC제형으로 변경될 예정이다.
이 시장에서는 위치선점이 매우 중요해보인다. 키트루다 역시 옵디보보다도 먼저 선점하였던 효과가 있어보인다.
이 부분은 미국에서는 옵디보보다 조금 더 빠르게 출시한 키트루다가 매출을 크게 앞질렀지만,
반면에 일본에서는 키트루다보다 먼저 출시한 옵디보의 매출이 더 좋았다는 점에서 살펴볼 수 있다.
그런 상황에서 만약 SC제형에서 늦어진다면? 그것도 많이?
생각하는 만큼 키트루다 SC의 수익성이 나지 않을 수 있다. 그러므로 시간 싸움이다.
사실, 이미 늦은 편이다. 할로자임과 연합한 옵디보SC는 이미 2024년 12월에 승인이 되었다. 올해 상반기에 출시된다.
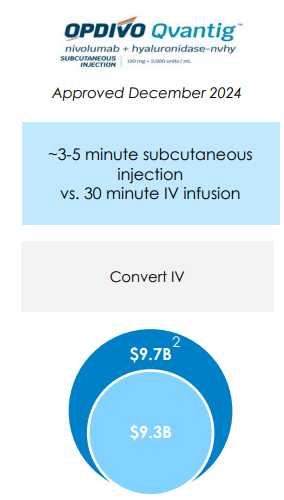
키트루다는 정상적인 루트를 밟는다면 올해 말 혹은 2026년 출시가 가능할 것이다.
이런 상황에서 소송에 휘말린다면 시장 선점을 놓칠 수 있다. 그리고 2028년 특허만료도 코앞이다.
키트루다는 머크 매출의 절반 이상을 차지하는 약물이기 때문에 문제가 심각해질 수 있다.

최근 25년 3월 7일 할로자임이 제출한 답변서이다. PDF 기준 108페이지 정도된다. 아래 내용은 그록을 통해 요약한 내용이다.
주요 논점 요약
Halozyme는 Merck의 PGR 신청이 여러 치명적인 결함을 가지고 있다고 주장하며, PTAB가 PGR 절차를 개시하지 말아야 한다고 촉구합니다. 아래는 문서의 핵심 주장과 이를 뒷받침하는 세부 논거를 정리한 내용입니다.
1. PGR 적격성 문제
주장: Merck가 '600 특허의 PGR 적격성을 입증하지 못했다.
근거:
PGR은 America Invents Act(AIA)에 따라 2013년 3월 16일 이후 유효 출원일(effective filing date)을 가진 특허에만 적용된다.
'600 특허는 2012년 12월 28일에 출원된 '731 신청서(비임시 신청서)에 우선권을 주장하며, 이는 AIA 이전 날짜다.
Merck는 '731 신청서를 2012년 출원일 기준으로 분석하지 않고, 2011년 날짜만을 기준으로 삼아 작성 설명(written description)과 실시 가능성(enablement)을 평가했다.
이는 법적으로 부적절하며, Merck는 특허가 2012년 출원일의 이익을 받을 수 없음을 입증하지 못했다.
결론: PGR 적격성 ...