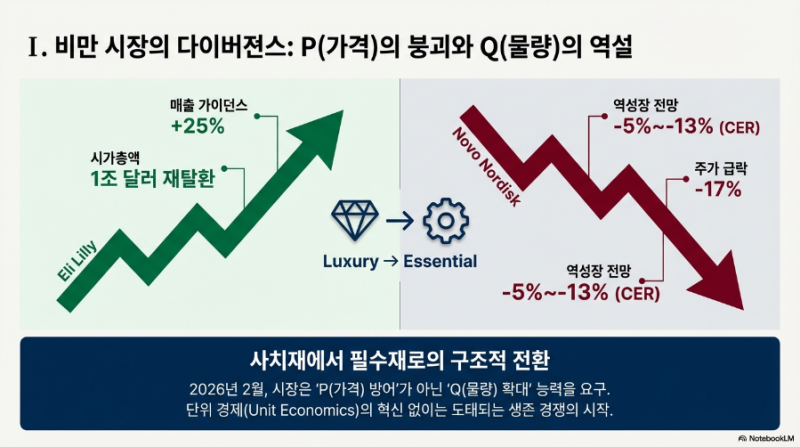
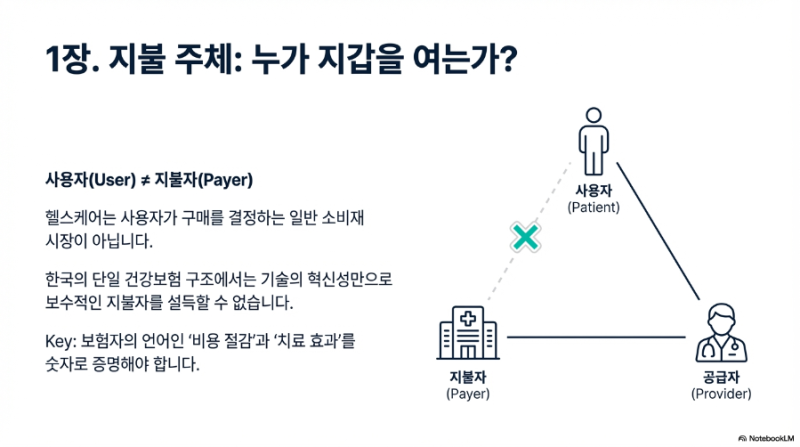
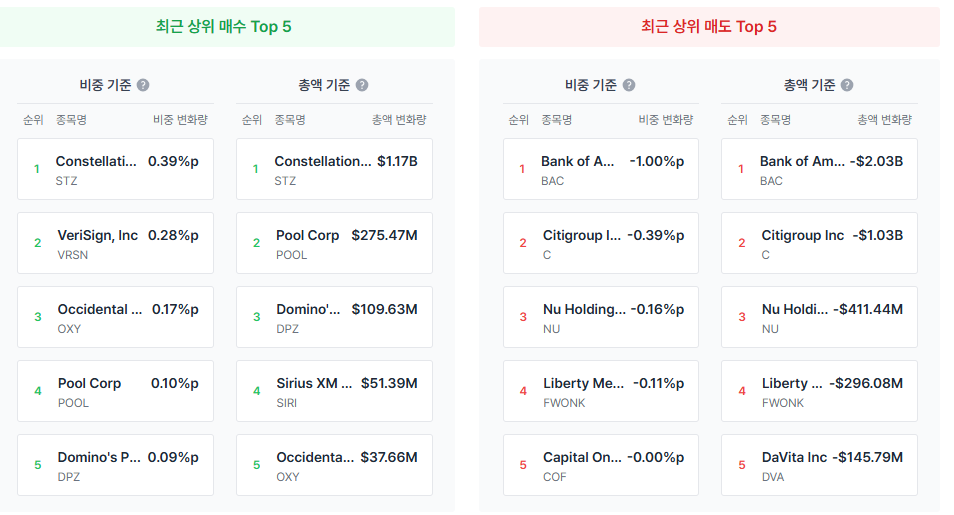
코스닥 입성 1주년을 맞이한 오름테라퓨틱스의 최근 주가 흐름이 지지부진하다. 지난 1년 간 주가 6배 상승이라는 기염을 토하며 시장의 찬사를 받던 기세가 한풀 꺾인 모양새다. 최근 발생한 조정의 트리거에 대해 시장은 두 가지 요인을 꼽는다. 첫째로는 상장 1주년 보호예수(Lock-up) 해제에 따른 오버행(Overhang) 리스크다. 초기 투자자들의 차익 실현 욕구가 시장에 잠재적 매도 물량으로 쏟아질 수 있다는 우려가 선반영되며 투자 심리를 억누르고 있다. 둘째로는 J.P. 모건 헬스케어 컨퍼런스 이후의 섹터 로테이션이다. 대형 이벤트 이후 바이오 섹터 전반에 차익 실현 매물이 출회되며, 그간 가파르게 상승했던 종목들을 중심으로 가격 조정이 이루어지고 있다는 것이다.
최근의 조정을 감안하더라도, 그간 오름테라퓨틱스가 보여준 저력은 분명하다. 과연 어떤 잠재력을 갖고 있기에 상장 후 폭발적인 주가 상승을 보여줬을까? 그리고 지금의 조정을 발판 삼아 다시 더욱 견고하게 일어설 수 있을까? 시장이 갖고 있는 '기대'와 '우려'가 혼재된 이 시점, 전문의 투자자로서 단순한 기대감을 배제하고 임상 데이터와 약리학적 기전을 바탕으로 이 기업의 본질을 냉정하게 해부하고자 한다.
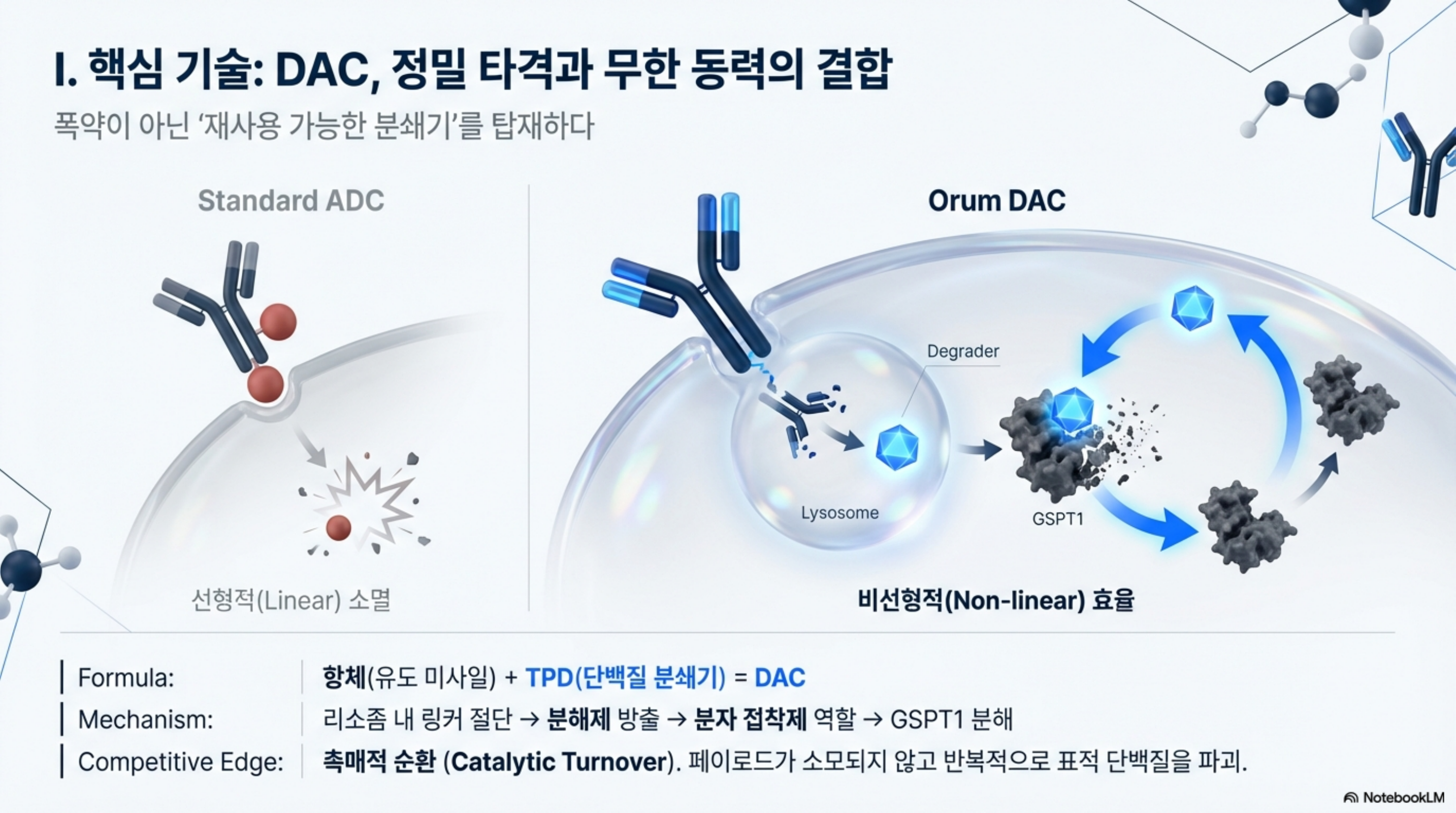
I. 핵심 기술 분석: DAC, 페이로드의 세대교체
오름테라퓨틱스의 핵심 파이프라인 가치를 평가하기 위해서는, 그들의 주된 약물 전달 모달리티인 DAC(Degrader-Antibody Conjugate)에 대해 알아야 한다. 직관적인 비유를 들자면, DAC는 암세포를 향하는 '정밀 타겟 유도 미사일(항체)'에 단순한 '폭약(독성 약물)' 대신 고성능 '단백질 분쇄기(Degrader)'를 탑재하여 공격하는 기술이다.
GSPT1 분해제를 탑재한 이 DAC의 작동 원리를 이해하기 위해서는, 표적 단백질인 GSPT1의 생리학적 역할과 이 단백질의 소실이 암세포에 미치는 치명적인 연쇄 반응을 먼저 살펴볼 필요가 있다.
1. GSPT1 분해, '번역 제동 장치' 제동을 통한 시스템 과부하
오름이 표적으로 삼은 GSPT1(G1 to S Phase Transition 1)은 인체 세포 내에서 단백질 합성 과정에서 리보솜(Ribosome)에 작용하는 번역 종결 인자(eRF3a)다. 리보솜은 아미노산을 붙여가며 단백질을 형성하는데, 적절한 순간에 여기서 멈추라는 신호를 내리는 역할을 GSPT1이 한다. 암세포의 경우 끊임없는 증식을 위해 다량의 단백질 합성이 일어나는데, 이 제동 장치인 GSPT1의 제거는 치명적인 결과를 초래한다.
GSPT1이 소실되면 리보솜이 멈춰야 할 시점을 인식하지 못하고 불필요한 아미노산을 계속 갖다 붙이는 '번역 오류(Translation Error)'가 발생한다. 정상적인 단백질이 아닌 불량 단백질(Misfolded protein)이 세포 내에 과적되면, 암세포는 통합 스트레스 반응(Integrated Stress Response, ISR)에 직면하게 된다. 결국 암세포는 이 시스템 과부하를 견디지 못하고 스스로 세포 사멸(Apoptosis) 스위치를 켜게 된다. 즉, 세포막을 찢거나 굶겨 죽이는 1차원적 항암이 아니라, 암세포 고유의 과잉 대사 시스템을 역이용해 자멸을 유도하는 고도화된 기전이다.
2. 선형적 반응을 넘어서는 비선형적 '촉매적 순환'
오름의 DAC는 암세포 표면의 특정 항원(HER2, CD33 등)을 정밀 타겟한 뒤, 세포 내부로 스스로를 밀어 넣는다(내재화). 이때 오름의 특수 링커 기술이 힘을 발휘한다. 혈류를 타고 이동할 때는 분해제가 밖으로 새지 않도록 불활성 상태로 유지하다가, 암세포 내부의 소화 기관인 리소좀에 도착해서야 비로소 링커가 끊어지며 진짜 무기인 분해제를 세포질로 방출한다.
세포 안으로 풀려난 분해제는 일종의 '분자 접착제(Molecular Glue)'가 된다. 세포 내 단백질 청소부 역할을 하는 효소인 'E3 리가아제(E3 Ligase)'와 암세포 생존에 필수적인 타깃 단백질 'GSPT1'을 결합시킨다. 두 단백질이 맞붙으면, E3 리가아제는 GSPT1 표면에 분해를 지시하는 꼬리표(유비퀴틴)를 연달아 붙이는데, 이 과정을 유비퀴틴화(Ubiquitination)라고 한다.
꼬리표가 붙은 GSPT1은 세포 내 단백질 분쇄기인 프로테아좀(Proteasome)으로 끌려가 산산조각이 난다. 이처럼 세포 본연의 단백질 분해 시스템을 이용해 질병의 원인이 되는 단백질만 원천적으로 분해해 버리는 신약 개발 방식을 바로 '표적 단백질 분해(TPD, Targeted Protein Degradation)' 기술이라고 부른다. 즉, 오름의 DAC는 정밀 유도 미사일(항체)에 바로 이 TPD를 탄두로 탑재한 것이다.
기존 ADC(항체-약물 접합체)와 오름의 DAC를 가르는 가장 결정적인 차이이자 임상적 해자는 바로 '페이로드(Payload)의 재사용성'에 있다. GSPT1이 분해될 때, TPD 분해제(페이로드)는 1회용으로 소모되지 않고 온전히 떨어져 나온다. 자유로워진 분해제는 또 다른 GSPT1을 찾아 끝없이 분해 시스템을 활성화시키는 '촉매적 순환(Catalytic Turnover)'을 시작한다.
목표물을 타격한 뒤 장렬히 소멸하여 선형적(Linear)인 용량-반응을 보이는 기존 1회용 독성 ADC와 달리, DAC의 경우 탑재된 TPD 분해제 한 개가 다량의 GSPT1을 연쇄적으로 파괴한다. 이러한 비선형적(Non-linear) 파괴력 덕분에, DAC는 이론상 극소량의 약물만으로도 암세포의 시스템에 치명적인 과부하를 일으킬 수 있는 것이다.
3. TPD² 플랫폼, 왜 오름인가?
글로벌 빅파마들이 오름테라퓨틱스의 TPD²(Dual-Precision TPD) 플랫폼에 주목하는 이유는 명확하다. 표적 단백질 분해(TPD) 분야의 오랜 난제였던 '치료 지수(Therapeutic Index)의 확장'에 ...